que es la tabla periodica
Los pesos atómicos
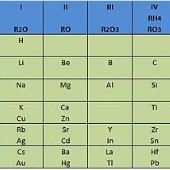
imagen de la tabla
Primeros intentos de sistematización
Ley de las octavas de Newlands
Tabla periódica de Mendeléyev
como se denominan las filas y las columnas en la tabla
Noción de elemento y propiedades periódicas
Descubrimiento de los elementos
historia
quien y en que año publico la primera versión de la tabla periódica
El químico inglés John Newlands produjo una serie de documentos de 1863 a 1866 y señaló que cuando los elementos se enumeran en orden de aumentar el peso atómico, las propiedades físicas y químicas similares se repiten a intervalos de ocho.n. 2 Ley de las octavas de Newlands 1 2 3 4 5 6 7 Li 6,9 Na 23,0 K 39,0 Be 9,0 Mg 24,3 Ca 40,0 B 10,8 Al 27,0 C 12,0 Si 28,1 N 14,0 P 31,0 O 16,0 S 32,1 F 19,0 Cl 35,5 Comparó esta periodicidad con las octavas de la música.2021 Esta llamada «ley de las octavas» fue ridiculizada por los contemporáneos de Newlands y la Chemical Society se negó a publicar su obra,22 porque dejaba de cumplirse a partir del calcio. Newlands fue sin embargo capaz de elaborar una tabla de los elementos y la utilizó para predecir la existencia de elementos faltantes, como el germanio.23 La Chemical Society solamente reconoció la importancia de sus descubrimientos cinco años después de que se le acreditaran a Mendeléyev,24 y posteriormente fue reconocido por la Royal Society, que le concedió a Newlands su más alta condecoración, la medalla Davy.[cita requerida] En 1867 Gustavus Hinrichs, un químico danés, publicó un sistema periódico en espiral sobre la base de los espectros, los pesos atómicos y otras similitudes químicas. Su trabajo fue considerado como idiosincrásico, ostentoso y laberíntico y esto puede haber llevado a que se desaconsejase su reconocimiento y aceptación.
A principios del siglo xix, John Dalton (1766-1844) desarrolló una concepción nueva del atomismo, a la que llegó gracias a sus estudios meteorológicos y de los gases de la atmósfera. Su principal aportación consistió en la formulación de un «atomismo químico» que permitía integrar la nueva definición de elemento realizada por Antoine Lavoisier (1743-1794) y las leyes ponderales de la química (proporciones definidas, proporciones múltiples, proporciones recíprocas). Dalton empleó los conocimientos sobre proporciones en las que reaccionaban las sustancias de su época y realizó algunas suposiciones sobre el modo como se combinaban los átomos de las mismas. Estableció como unidad de referencia la masa de un átomo de hidrógeno (aunque se sugirieron otros en esos años) y refirió el resto de los valores a esta unidad, por lo que pudo construir un sistema de masas atómicas relativas. Por ejemplo, en el caso del oxígeno, Dalton partió de la suposición de que el agua era un compuesto binario, formado por un átomo de hidrógeno y otro de oxígeno. No tenía ningún modo de comprobar este punto, por lo que tuvo que aceptar esta posibilidad como una hipótesis a priori. Dalton sabía que una parte de hidrógeno se combinaba con siete partes (ocho, afirmaríamos en la actualidad) de oxígeno para producir agua. Por lo tanto, si la combinación se producía átomo a átomo, es decir, un átomo de hidrógeno se combinaba con un átomo de oxígeno, la relación entre las masas de estos átomos debía ser 1:7 (o 1:8 se calcularía en la actualidad). El resultado fue la primera tabla de masas atómicas relativas (o pesos atómicos, como los llamaba Dalton), que fue posteriormente modificada y desarrollada en los años posteriores. Las inexactitudes antes mencionadas dieron lugar a toda una serie de polémicas y disparidades respecto a las fórmulas y los pesos atómicos, que solo comenzarían a superarse, aunque no totalmente, en el congreso de Karlsruhe en 1860.
La historia de la tabla periódica está íntimamente relacionada con varios aspectos del desarrollo de la química y la física: El descubrimiento de los elementos de la tabla periódica. El estudio de las propiedades comunes y la clasificación de los elementos. La noción de masa atómica (inicialmente denominada «peso atómico») y, posteriormente, ya en el siglo xx, número atómico. Las relaciones entre la masa atómica (y, más adelante, el número atómico) y las propiedades periódicas de los elementos y la aparición de nuevos elementos.
Aunque algunos elementos como el oro (Au), plata (Ag), cobre (Cu), plomo (Pb) y mercurio (Hg) ya eran conocidos desde la antigüedad, el primer descubrimiento científico de un elemento ocurrió en el siglo xvii, cuando el alquimista Henning Brand descubrió el fósforo (P).9 En el siglo xviii se conocieron numerosos nuevos elementos, los más importantes de los cuales fueron los gases, con el desarrollo de la química neumática: oxígeno (O), hidrógeno (H) y nitrógeno (N). También se consolidó en esos años la nueva concepción de elemento, que condujo a Antoine Lavoisier a escribir su famosa lista de sustancias simples, donde aparecían 33 elementos. A principios del siglo xix, la aplicación de la pila eléctrica al estudio de fenómenos químicos condujo al descubrimiento de nuevos elementos, como los metales alcalinos y alcalino-térreos, sobre todo gracias a los trabajos de Humphry Davy. En 1830 ya se conocían 55 elementos. Posteriormente, a mediados del siglo xix, con la invención del espectroscopio, se descubrieron nuevos elementos, muchos de ellos nombrados por el color de sus líneas espectrales características: cesio (Cs, del latín caesĭus, azul), talio (Tl, de tallo, por su color verde), rubidio (Rb, rojo), etc. Durante el siglo xx, la investigación en los procesos radioactivos llevó al descubrimiento en cascada de una serie de elementos pesados (casi siempre sustancias artificiales sintetizadas en laboratorio, con periodos de vida estable muy cortos), hasta alcanzar la cifra de 118 elementos con denominación oficialmente aceptados por la IUPAC en noviembre de 2016
Dmitri Mendeléyev publicó en 1869 la primera versión de tabla periódica que fue ampliamente reconocida. La desarrolló para ilustrar tendencias periódicas en las propiedades de los elementos entonces conocidos, al ordenar los elementos basándose en sus propiedades químicas,3 si bien Julius Lothar Meyer, trabajando por separado, llevó a cabo un ordenamiento a partir de las propiedades físicas de los átomos.4 Mendeléyev también pronosticó algunas propiedades de elementos entonces desconocidos que anticipó que ocuparían los lugares vacíos en su tabla. Posteriormente se demostró que la mayoría de sus predicciones eran correctas cuando se descubrieron los elementos en cuestión.
En 1789 Antoine Lavoisier publicó una lista de 33 elementos químicos, agrupándolos en gases, metales, no metales y tierras.10 Aunque muy práctica y todavía funcional en la tabla periódica moderna, fue rechazada debido a que había muchas diferencias tanto en las propiedades físicas como en las químicas.[cita requerida] Los químicos pasaron el siglo siguiente buscando un esquema de clasificación más preciso. Uno de los primeros intentos para agrupar los elementos de propiedades análogas y relacionarlos con los pesos atómicos se debe al químico alemán Johann Wolfgang Döbereiner (1780-1849) quien en 1817 puso de manifiesto el notable parecido que existía entre las propiedades de ciertos grupos de tres elementos, con una variación gradual del primero al último. Posteriormente (1827) señaló la existencia de otros grupos en los que se daba la misma relación —cloro, bromo y yodo; azufre, selenio y telurio; litio, sodio y potasio—. Tríadas de Döbereiner Litio LiCl LiOH Calcio CaCl2 CaSO4 Azufre H2S SO2 Sodio NaCl NaOH Estroncio SrCl2 SrSO4 Selenio H2Se SeO2 Potasio KCl KOH Bario BaCl2 BaSO4 Telurio H2Te TeO2 A estos grupos de tres elementos se los denominó tríadas. Al clasificarlas, Döbereiner explicaba que el peso atómico promedio de los pesos de los elementos extremos, es parecido al del elemento en medio.11 Esto se conoció como la ley de Tríadas.12 Por ejemplo, para la tríada cloro-bromo-yodo, los pesos atómicos son respectivamente 36, 80 y 127; el promedio es 81, que es aproximadamente 80; el elemento con el peso atómico aproximado a 80 es el bromo, lo cual hace que concuerde con el aparente ordenamiento de tríadas. El químico alemán Leopold Gmelin trabajó con este sistema, y en 1843 había identificado diez tríadas, tres grupos de cuatro, y un grupo de cinco. Jean-Baptiste Dumas publicó el trabajo en 1857 que describe las relaciones entre los diversos grupos de metales. Aunque los diversos químicos fueron capaces de identificar las relaciones entre pequeños grupos de elementos, aún tenían que construir un esquema que los abarcara a todos.
Las filas de la tabla se denominan períodos y las columnas grupos. Algunos grupos tienen nombres. Así por ejemplo el grupo 17 es el de los halógenos y el grupo 18 el de los gases nobles. La tabla también se divide en cuatro bloques con algunas propiedades químicas similares. Debido a que las posiciones están ordenadas, se puede utilizar la tabla para obtener relaciones entre las propiedades de los elementos, o pronosticar propiedades de elementos nuevos todavía no descubiertos o sintetizados. La tabla periódica proporciona un marco útil para analizar el comportamiento químico y es ampliamente utilizada en química y otras ciencias.
es una disposición de los elementos químicos en forma de tabla, ordenados por su número atómico (número de protones), por su configuración de electrones y sus propiedades químicas. Este ordenamiento muestra tendencias periódicas, como elementos con comportamiento similar en la misma columna. En palabras de Theodor Benfey, la tabla y la ley periódica «son el corazón de la química —comparables a la teoría de la evolución en biología (que sucedió al concepto de la Gran Cadena del Ser), y a las leyes de la termodinámica en la física clásica

Lógicamente, un requisito previo necesario a la construcción de la tabla periódica era el descubrimiento de un número suficiente de elementos individuales, que hiciera posible encontrar alguna pauta en comportamiento químico y sus propiedades. Durante los siguientes dos siglos se fue adquiriendo un mayor conocimiento sobre estas propiedades, así como descubriendo muchos elementos nuevos. La palabra «elemento» procede de la ciencia griega, pero su noción moderna apareció a lo largo del siglo xvii, aunque no existe un consenso claro respecto al proceso que condujo a su consolidación y uso generalizado. Algunos autores citan como precedente la frase de Robert Boyle en su famosa obra El químico escéptico, donde denomina elementos «ciertos cuerpos primitivos y simples que no están formados por otros cuerpos, ni unos de otros, y que son los ingredientes de que se componen inmediatamente y en que se resuelven en último término todos los cuerpos perfectamente mixtos». En realidad, esa frase aparece en el contexto de la crítica de Robert Boyle a los cuatro elementos aristotélicos. A lo largo del siglo xviii, las tablas de afinidad recogieron un nuevo modo de entender la composición química, que aparece claramente expuesto por Lavoisier en su obra Tratado elemental de química. Todo ello condujo a diferenciar en primer lugar qué sustancias de las conocidas hasta ese momento eran elementos químicos, cuáles eran sus propiedades y cómo aislarlas. El descubrimiento de gran cantidad de elementos nuevos, así como el estudio de sus propiedades, pusieron de manifiesto algunas semejanzas entre ellos, lo que aumentó el interés de los químicos por buscar algún tipo de clasificación.