formula molecular
historia de los fenoles
formula semidesarrollada
imagen del fenol
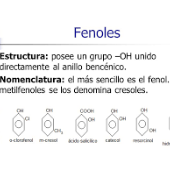
formula estructural
usos de los fenoles
riesgos
que son los fenoles
apariencia
obtencion de los fenoles
Industrialmente se obtiene mediante oxidación (con aire) de cumeno (isopropil benceno) a hidroperóxido de cumeno, que posteriormente, en presencia de un ácido, se encinde en fenol y acetona, que se separan por destilación.
El fenol se evapora más lentamente que el agua y una pequeña cantidad puede formar una solución con agua. Se puede detectar el sabor y el olor del fenol a niveles más bajos que los asociados con efectos nocivos. El fenol se inflama fácilmente, es corrosivo y sus gases son explosivos en contacto con fuego. De ser ingerido en altas concentraciones, puede causar envenenamiento, vómitos, decoloración de la piel e irritación respiratoria. Era la sustancia utilizada en los campos de concentración nazis desde agosto de 1941 para disponer de las llamadas "inyecciones letales" (inyección de fenol de 10 cm³). Desafortunadamente es uno de los principales desechos de industrias carboníferas y petroquímicas; como consecuencia el fenol entra en contacto con cloro en fuentes de agua tratadas para consumo humano, y forma compuestos fenilclorados, muy solubles y citotóxicos por su facilidad para atravesar membranas celulares.
El fenol se usa principalmente en la producción de resinas fenólicas. También se usa en la manufactura de nylon y otras fibras sintéticas. El fenol es muy utilizado en la industria química, farmacéutica y clínica como un potente fungicida, bactericida, sanitizante, antiséptico y desinfectante, también para producir agroquímicos, bisfenol A (materia prima para producir resinas epoxi y policarbonatos), en el proceso de fabricación de ácido acetilsalicílico (aspirina) y en preparaciones médicas como enjuagues bucales y pastillas para el dolor de garganta
C6H5OH ó φOH
C6H6O
son compuestos orgánicos aromáticos que contienen el grupo hidroxilo como su grupo funcional. ... Las concentraciones naturales de compuestos fenólicos son usualmente inferiores a 1 µg/l y los compuestos más frecuentemente identificados son fenol, cresol y los ácidos siríngico, vainíllico y p-hidroxibenzoico
El fenol fue descubierto en 1834 por Friedrich Ferdinand Runge, que lo extrajo (en forma impura) a partir del alquitrán de hulla.23 Runge llamó al fenol "Karbolsäure" (carbón-aceite-ácido, el ácido carbólico). El alquitrán de hulla se mantuvo como fuente primaria hasta el desarrollo de la industria petroquímica. En 1841, el químico francés Auguste Laurent obtuvo fenol en forma pura.4 En 1836, Auguste Laurent acuñó el nombre de "phène" para el benceno;5 esta es la raíz de la palabra "fenol" y "fenilo". En 1843, el químico francés Charles Gerhardt acuñó el nombre de "phénol"
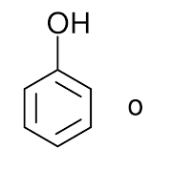
Blanco-incoloro