El cunjunto de números cuánticos (3,2,-3, +1/2) tiene un error debido a que
Afirma que: dos electrones en un átomo no pueden tener los mismos números cuánticos iguales, este principio lo estableció
Los números cuánticos que representan a un electrón que se encuentra ubicado en el periodo 5d son
El principio que establece que los orbitales con igual nivel de energía ( se refiere a orbitales con el mismo número cuántico n y el mismo número cuántico l), se llenan progresivamente de manera que siempre exista un mayor número de electrones desapareados, se conoce como
Un electrón que se encuentra en el nivel 2p, tendría el siguiente conjunto de números cuánticos
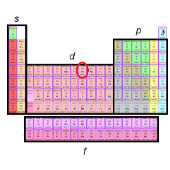
Los números cuánticos (4,2,0, -1/2) corresponde al elemento mostrado en la siguiente tabla periódica
Los números cuánticos (4 ,2,-1,-1/2) corresponden al elemento mostrado en la siguiente tabla periódica
En principio que nos dice primero se llenan los orbitales de menos energía y luego los de mayor energía es
En el siguiente conjunto de números cuánticos (2,2,-1,+1/2) hay un error porque

El número cuántico magnífico puede tomar un valor comprendido entre -l y l

(5, 2, -1, -1/2)
En número cuántica azimutal se calcula restándole una unidad al número cuántico principal
Principio de Aufbau
Principio de llenado de Hund
(2,1,0, +1/2)